P9 B. Warscheid
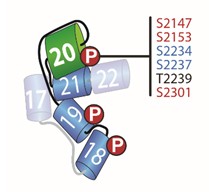
Regulation von Kinase-Substrat-Netzwerken in Skelettmuskelzellen unter mechanischen Stress
Eine koordinierte und zeitabhängige Regulation von Signaltransduktionswegen, welche zusammen ein komplexes Signalnetzwerk bilden, ist essentiell, um den mechanischen Anforderungen des kontrahierenden Skelettmuskels gerecht zu werden. Proteinphosphorylierung spielt eine fundamentale Rolle für die durch mechanische Belastung hervorgerufenen molekularen Reaktionen. Diese Phosphorylierungsereignisse werden von Proteinkinasen eng kontrolliert und bestimmen zelluläre Antworten. In den letzten Jahren sind die Datensätze zu Proteinphosphorylierungen deutlich angestiegen. Für die meisten der identifizierten Phosphorylierungsstellen existieren jedoch keine Annotationen über upstream agierende Kinasen und/oder funktionelle Daten.
Im Rahmen dieses Projektes werden wir neue Erkenntnisse über Kinase-Substrat-Beziehungen als Reaktion auf mechanischen Stress generieren, indem wir das sogenannte "dunkle Phosphoproteom" näher beleuchten. Wir werden zeitaufgelöste Profile der Aktivitäten zentraler Kinasen von Skelettmuskelzellen, die mechanischem Stress ausgesetzt sind, erstellen. Durch integrative, quantitative Phosphoproteomanalysen werden wir in kultivierten, kontrahierenden Skelettmyotuben der Maus und humanen Skelettmuskeln global die Signalnetzwerke in Abhängigkeit von mechanischem Stress untersuchen. In einem komplementären Ansatz werden wir durch pharmakologische Interventionen physiologische Substrate der beiden zentralen Kinasen Proteinkinase B und Proteinkinase C alpha bei mechanischem Stress untersuchen. Neue Substratstellen, die in Proteinen mit Schlüsselfunktionen bei der Antwort auf mechanischen Stress identifiziert wurden, werden dann in in vitro und in cellulo Kinaseassays validiert werden. In unseren funktionellen Analysen werden wir aus unserem Wissen über Filamin C Phosphorylierung gezielt Nutzen ziehen, um kinasekontrollierte Mechanismen, die der Modulation von Filamin C-Dynamik, -Abbau, -Interaktionen und seiner Eigenschaft als Kraft-Sensor zugrunde liegen, zu identifizieren. Insgesamt betrachtet, wird unsere Arbeit stressabhängige Kinase-Substrat-Beziehungen und regulatorische Mechanismen aufdecken und beleuchten, wie Skelettmuskelzellen mit mechanischem Stress fertig werden und darauf antworten.
Kontakt
Prof. Dr. Bettina Warscheid
Am Hubland
97074 Würzburg